- 2018年诺贝尔生理或医学奖揭晓,癌症免疫治疗摘桂冠!
-
 admin
admin
 本网站
本网站
 2018-10-10
2018-10-10
 1500
[ 关闭窗口 ]
1500
[ 关闭窗口 ]
当地时间10月1日上午11时30分(北京时间10月1日下午5时30分)2018年度诺贝尔生理或医学奖获得者揭晓。今年该奖项的获得者分别是美国得州大学奥斯汀分校免疫学家詹姆斯·艾利森(James P. Allision)和日本京都大学教授本庶佑(Tasuku Honjo),以表彰他们发现了抑制免疫调节的癌症疗法。


获奖者:James P.Allison和Tasuku Honjo
获奖原因:发现免疫检查点抑制癌症疗法,成为对抗癌症的一个里程碑
重要意义:艾利森和本庶佑证实了抑制免疫系统制动器的不同策略如何被用于癌症治疗。两位科学家在癌症免疫治疗领域取得了开拓性贡献,改变了人类对抗癌症的格局,免疫疗法有望成为癌症治疗的新希望,其重要发现构成了对抗癌症的一个里程碑。
抗癌之路
癌症包括许多不同的疾病,其特征都是异常细胞不受控制的增殖,并会扩散到健康的器官和组织。有许多治疗癌症的方法可供选择,包括手术、放疗和其他策略,其中一些方法曾获得诺贝尔奖。这些方法包括激素治疗前列腺癌(Huggins,1966)、化疗(Elion和Hitchins,1988)和骨髓移植治疗白血病(Thomas,1990)。然而,晚期癌症仍然非常难以治疗,迫切需要新的治疗策略。
19世纪末20世纪初,一种新策略出现了,即免疫系统的激活或可攻击肿瘤细胞。科学家尝试用细菌感染病人来激活防御系统。这些努力只产生了有限的效果,但这一策略的变体今天被用于膀胱癌的治疗。人们意识到需要更多的知识。许多科学家进行了大量深入的基础研究,发现了调节免疫的基本机制,并展示了免疫系统如何识别癌细胞。尽管取得了显著的科学进展,但研究出可推广的抗癌新策略的尝试被证明仍很困难。
癌症每年导致上百万人死亡,是人类面临的最大健康挑战之一。通过刺激人类免疫系统的内在能力攻击肿瘤细胞,今年的诺贝尔奖获得者奖励了针对癌症疗法的全新策略。

詹姆斯·艾利森

本庶佑
两位获奖者
詹姆斯·艾利森研究的是一种作为免疫系统制动器的已知蛋白。他意识到释放该制动器并由此释放人体免疫细胞攻击肿瘤的潜力。随后,他将这一概念发展成全新的治疗肿瘤患者的方法。
本庶佑发现了免疫细胞上的一种蛋白质。在仔细探究其功能后,本庶佑最终发现它也可以作为制动器,只不过作用机制不同。基于该发现的疗法被证实在对抗癌症时非常有效。
詹姆斯·艾利森教授是癌症免疫疗法的先驱之一,也被称“CTLA-4抗体Yervoy之父”。作为现代肿瘤免疫治疗的奠基人之一,在研究T细胞反应的调节和癌症免疫治疗策略有着杰出贡献,确定了T细胞受体结构,证实CTLA-4通过对抗 CD28介导的共同刺激抑制T细胞活化。
Tasuku Honjo教授是来自日本的医学家、美国国家科学院外籍院士。1992年,Tasuku Honjo发现T细胞抑制受体PD-1,2013年依此开创了癌症免疫疗法,功绩名列《Science》年度十大科学突破之首。Tasuku Honjo是德国医学最高奖罗伯·柯霍奖的“科霍奖”得主,被誉为“最接近诺贝尔奖的日本人之一”。
事实上,艾利森院士很早就在考虑能不能用免疫系统攻击癌症——找到肿瘤细胞逃避免疫攻击的机制,如果能防止免疫系统的关闭就可以消除肿瘤。这就是将CTLA-4应用到癌症治疗上的想法的来源。之后的实验很成功,注射了CTLA-4的抗体后,几乎所有的小鼠肿瘤都消除了。
免疫系统内的“加速器”和“制动器”
人们免疫系统的基本属性是区分“自我”和“非自我”的能力,这样入侵的细菌、病毒和其他危险就可以被攻击和消除。T细胞(一种白细胞)是这一防御的关键。
研究表明,T细胞具有受体,可以与非自体结构结合,这种相互作用会触发免疫系统进行防御。但作为T细胞加速器的其他蛋白质也需要触发全面的免疫反应。
许多科学家对这一重要的基础研究做出了贡献,他们还发现了可对T细胞起到“制动”作用的其他蛋白质,可抑制免疫激活。“加速器”和“制动器”之间这种复杂的平衡对于严格控制来说必不可少。它可以确保免疫系统充分参与到攻击外来微生物中,同时避免过度激活,从而导致健康细胞和组织的自身免疫破坏。
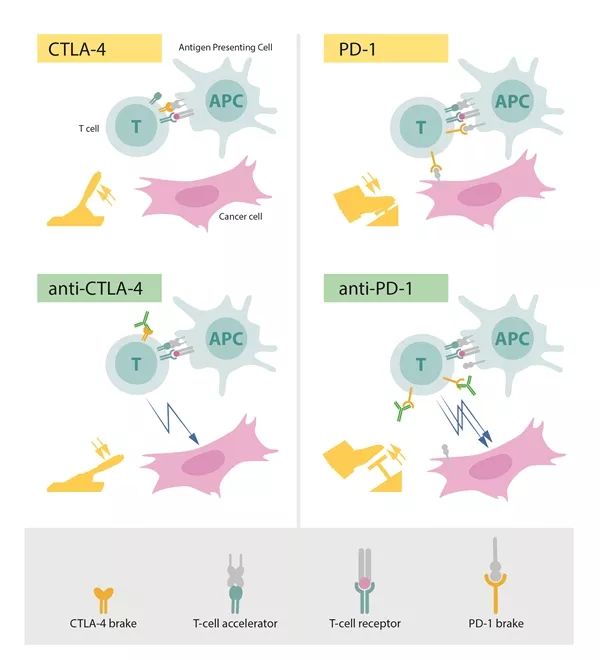
图:左上:T细胞的激活需要T细胞受体结合到其他“非自我”免疫细胞结构。作为T细胞“加速器”的蛋白质对于T细胞的激活也是必需的。CTLA- 4对T细胞起到制动作用,可抑制“加速器”的功能。
左下:针对CTLA-4的抗体(绿色)阻断了制动器的功能,导致T细胞激活并攻击癌细胞。右上:PD-1是另一种抑制T细胞激活的T细胞“制动器”。右下:PD-1抗体抑制“制动器”的功能,导致T细胞激活并对癌细胞进行高效攻击。
上世纪90年代,在位于加州大学伯克利分校的实验室,艾利森研究了T细胞蛋白CTLA-4。他是观察到CTLA-4是T细胞“制动器”的若干科学家之一。其他研究团队利用该机制探寻治疗自体免疫疾病的方法,但艾利森的想法完全不同。他开发出一种可同CTLA-4结合并抑制其功能的抗体。
现在,他打算研究“封锁”CTLA-4能否使T细胞脱离“制动”并且释放免疫系统攻击癌症细胞。艾利森和合作者在1994年底开展了第一次试验。让他们兴奋的是,试验在圣诞节假期便很快被重复出来。研究结果非常惊人。患有癌症的小鼠被利用抑制“制动器”并且释放抗肿瘤T细胞活性的抗体疗法得以治疗。尽管医药产业界对此兴趣不大,但·艾利森继续致力于将该策略发展成针对人类的疗法。颇有前景的研究结果很快在若干研究组出现。2010年,一种重要临床研究证实了该疗法在治疗晚期黑色素瘤患者时表现出的显著效果。在一些病人身上,残存的癌症迹象消失了。这些惊人的效果此前从未在该患者群体中出现过。
未来:进一步降低免疫治疗的副作用
艾利森院士认为免疫治疗的副作用在癌症治疗中远远不是问题。他们正设法降低副作用,现在所做的是对副作用的早期识别和早期处理。但是世界上没有完美的治疗方法。另外,降低副作用的方法还可以采取比如调整抗体的量,进行局部递送等等。而且一些措施已经显示了有效性。
来源:生物探索、人工智能学家、网络

 应用案例
应用案例 细胞学院
细胞学院 关于我们
关于我们 关注微信
关注微信